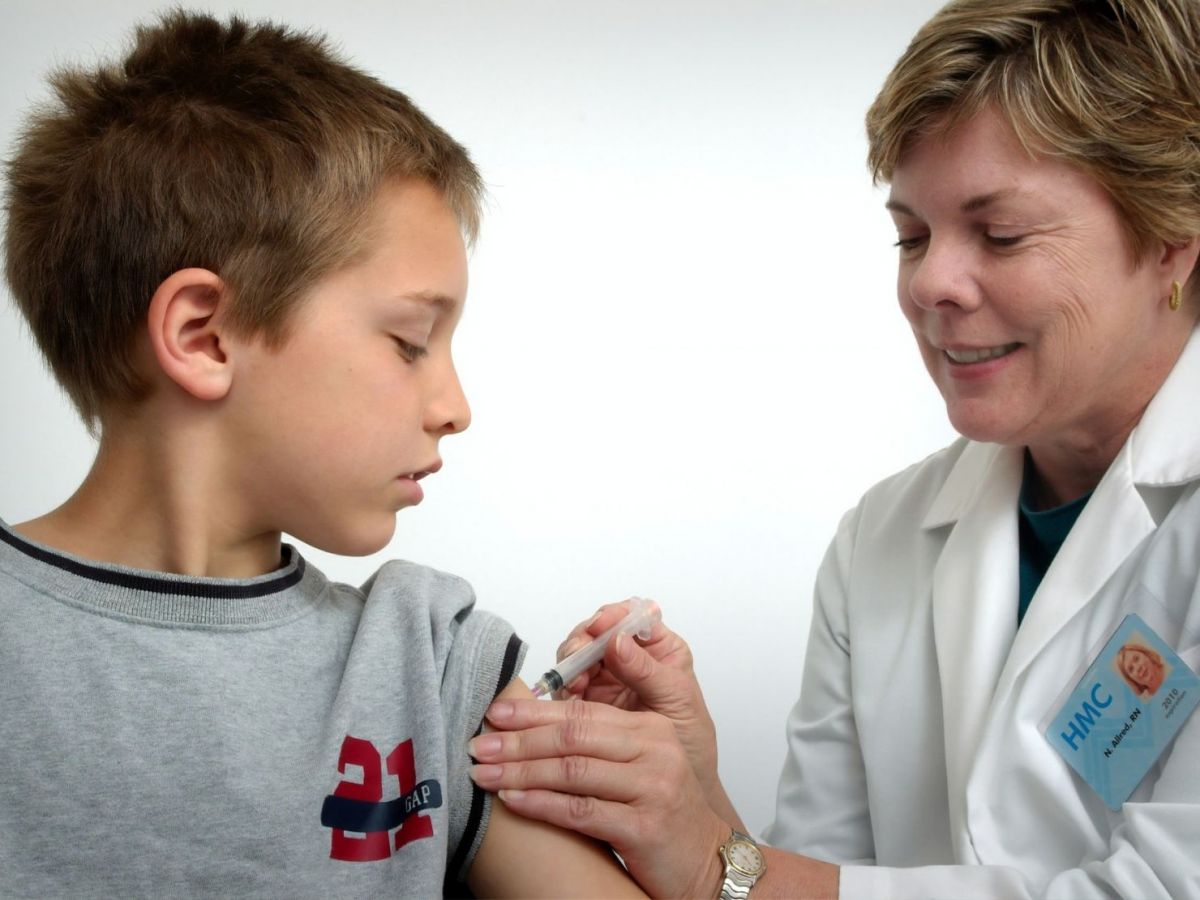
La vacuna Covid-19 Comirnaty está actualmente autorizada para su uso en personas de 12 años o más, y contiene una molécula denominada ARN mensajero (ARNm) con instrucciones para producir una proteína presente de forma natural en el SARS-CoV-2 y preparar al organismo para defenderse del virus causante del covid-19.
El Comité de Medicamentos de Uso Humano (CHMP) de la EMA revisará los datos sobre la vacuna, incluidos los resultados de un estudio clínico en curso en el que participan niños de entre cinco y once años, para decidir si recomienda o no la ampliación de la vacuna para su uso.
El dictamen del CHMP se transmitirá después a la Comisión Europea, que emitirá una decisión final.
La vacuna de Pfizer/BioNTech recibió una autorización de comercialización condicional en diciembre de 2020, siendo una de las cuatro que se administran en la Unión Europea, junto con Moderna, AstraZeneca y la vacuna de dosis única de Janssen.